強塩基性陰イオン交換樹脂
強塩基性陰イオン交換樹脂の概要
陰イオン交換樹脂は、官能基としてアミノ基を導入したイオン交換樹脂でClイオン、SO4イオンのような陰イオンを交換することができます。官能基であるアミンの塩基性の強さにより強塩基性陰イオン交換樹脂と弱塩基性陰イオン交換樹脂の2種類に分けられます。
四級アンモニウム基を持つイオン交換樹脂は、NaOH、KOHなどの強アルカリと同様に解離して強い塩基性を示し、強塩基性陰性イオン交換樹脂と呼ばれています。
強塩基性陰イオン交換樹脂の官能基は、強塩基性なため酸性だけでなくアルカリ性溶液の中でも解離します。
そのため、下記の反応のように鉱酸だけなく、NaClなどの中性塩もイオン交換することが出来ます。その他、水溶液中に存在する珪酸(シリカ)、炭酸などの弱酸も交換捕捉できます。 このように強塩基性陰イオン交換樹脂は、全pH領域でイオン交換性を持ちます。
R-N・OH + NaCl → R-N・Cl + NaOH
R-N・OH + HCl → R-N・Cl + H2O
R-N・OH + SiO2 → R-N・HSiO3
R-N・OH + HCl → R-N・Cl + H2O
R-N・OH + SiO2 → R-N・HSiO3
(Rはイオン交換樹脂の母体を示します。)
強塩基性陰イオン交換樹脂の再生は、通常約4%のNaOH水溶液で行ないます。塩基性の低いNH4OHでは殆ど再生できません。
以下に強塩基性陰イオン交換樹脂Cl形の再生時の反応式を示します。
R-N・Cl + NaOH → R-N・OH + NaCl
強塩基性陰イオン交換樹脂の再生は、官能基が強塩基性なため強酸性陽イオン交換樹脂と同様に再生しにくく、実用的には理論化学当量の数倍の再生剤が必要となります。
強塩基性陰イオン交換樹脂のI型とII型の比較
強塩基性陰イオン交換樹脂は、トリメチルアンモニウム基を持つⅠ型とジメチルエタノールアンモニウム基を持つⅡ型の塩基度の異なる2種類があります。
- Ⅰ型は塩基度が最も高く、陰イオンを強く吸着出来ることから高純度の脱塩水を得たい場合に使用されます。再生は、吸着力が強いため大量の再生剤が必要となります。
- Ⅱ型はⅠ型より塩基度が低いため、得られる脱塩水の水質はⅠ型より劣りますが、その分再生剤の使用量を減らすことが出来ます。
強塩基性陰イオン交換樹脂の化学構造
1)強塩基性陰イオン交換樹脂Ⅰ型の構造
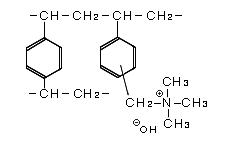
2)強塩基性陰イオン交換樹脂Ⅱ型の構造
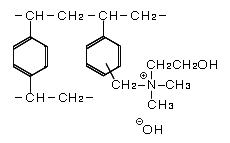
強塩基性陰イオン交換樹脂一覧
| Type | Product Name | Remarks |
|---|---|---|
| SBA | DIAION™ NSA100 | ※ |
| DIAION™ SA10A | ||
| DIAION™ SA10AL | ||
| DIAION™ SA10ALLP | Anti-clumping | |
| DIAION™ SA10AOH | ||
| DIAION™ SA10AP | Anti-clumping | |
| DIAION™ SA10DL | ||
| DIAION™ SA11A | ||
| DIAION™ SA11AL | ||
| DIAION™ SA12A | ||
| DIAION™ SA12AL | ||
| DIAION™ SA12ALL | ||
| DIAION™ SA20A | ||
| DIAION™ SA20ALL | ||
| DIAION™ SA20ALLP | Anti-clumping | |
| DIAION™ SA20AP | Anti-clumping | |
| DIAION™ SA20AP2 | Anti-clumping | |
| DIAION™ SAF11AL | Anti-clumping | |
| DIAION™ SANUPB | Anti-clumping | |
| DIAION™ SAT10L | Anti-clumping | |
| DIAION™ SAT20L | Anti-clumping | |
| DIAION™ UMA130J | Anti-clumping | |
| DIAION™ UBA100 | ||
| DIAION™ UBA100OH | ||
| DIAION™ UBA100OHUP | ||
| DIAION™ UBA120 | ||
| DIAION™ UBA120A | ||
| DIAION™ UBA120OH | ||
| DIAION™ UBA120OHUP | ||
| DIAION™ UBA150 | ||
| DIAION™ UBA200 | ||
| DIAION™ PA306S | ||
| DIAION™ PA308 | ||
| DIAION™ PA308L | ||
| DIAION™ PA312 | ||
| DIAION™ PA312L | ||
| DIAION™ PA312LOH | ||
| DIAION™ PA312LTUMB | ||
| DIAION™ PA316 | ||
| DIAION™ PA316L | ||
| DIAION™ PA318L | ||
| DIAION™ PA408 | ||
| DIAION™ PA412 | ||
| DIAION™ PA418 | ||
| DIAION™ PA418L | ||
| DIAION™ PA418LL | ||
| DIAION™ PAF308L | ||
| DIAION™ HPA25M | ||
| DIAION™ HPA512L | ||
| DIAION™ HPA716 | ※ | |
| Relite™ JA450 | ||
| Relite™ JA810 |
※ 最低販売数量に制限有。お問い合わせください
